招募中!上海昂昇生物与仁济医院合作开展糖尿病ED临床研究,现招募志愿者
2025年2月,上海昂昇生物医药科技有限公司联合上海交通大学医学院附属仁济医院即将开展一项前沿探索性临床研究,旨在为2型糖尿病合并中、重度勃起功能障碍(ED)患者带来新的治疗希望。
本次临床试验由上海仁济医院男科主任医师兼昂昇首席临床专家卢慕峻教授负责。采用由昂昇生物开发的Astem-101人脐带间充质干细胞(hUC-MSCs)注射液,为那些长期受常规PDE5i(如他达拉非或西地那非)治疗无效的患者提供一种全新的治疗思路。

卢慕峻教授介绍
一、研究背景
2型糖尿病与勃起功能障碍往往“联手”给男性带来双重困扰,影响生活质量和心理健康。尽管市面上已有一定疗效的PDE5i类药物,但对部分患者来说,治疗效果却不尽如人意。
为此,上海昂昇生物联合仁济医院的专家团队启动了这项非随机、开放、单臂的探索性临床试验——初步探索Astem-101人脐带间充质干细胞注射液用于经PDE5i规范治疗3个月无效的2型糖尿病合并中、重度勃起功能障碍(ED)的耐受性、安全性和有效性。
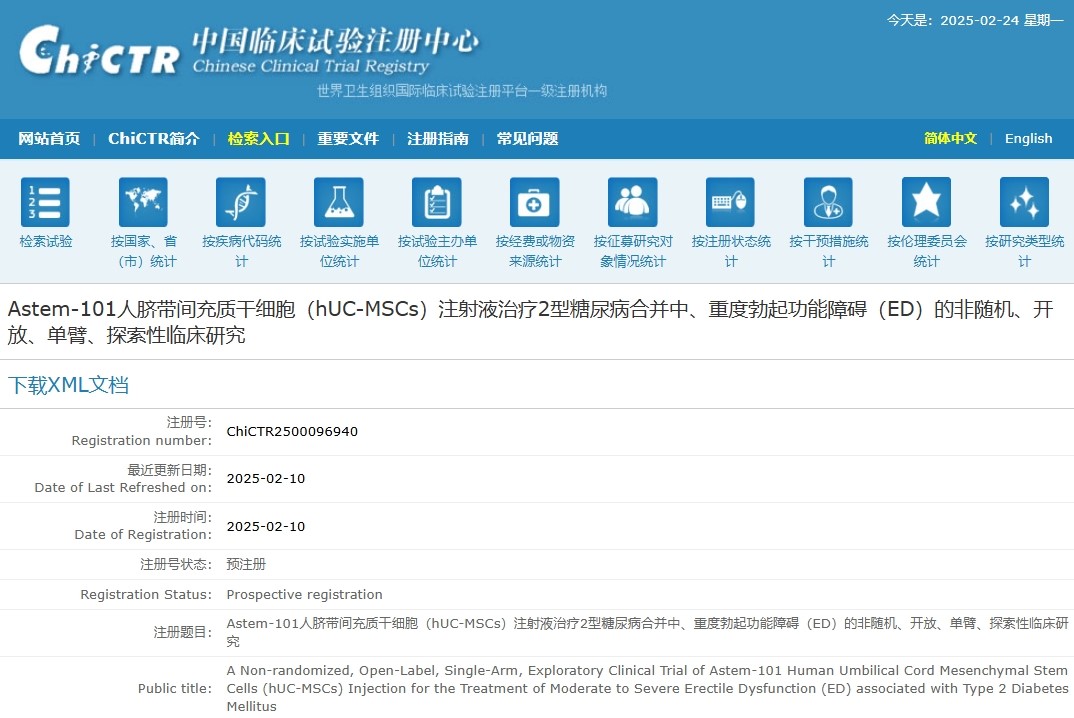
截图来源:中国临床试验注册中心
二、研究设计
本研究分为两个阶段,第一阶段将设置低、中、高三种剂量单次给药组,每组各6名受试者,筛选给药的最佳剂量水平;第二阶段则将在第一阶段基础上,选取最佳剂量方案,采用间隔4周注射一次,共两次的给药方式验证治疗的安全性和有效性。
整个试验自2023年9月6日启动,预计将持续至2028年8月24日,患者征募时间从2025年3月29日至2028年7月4日。
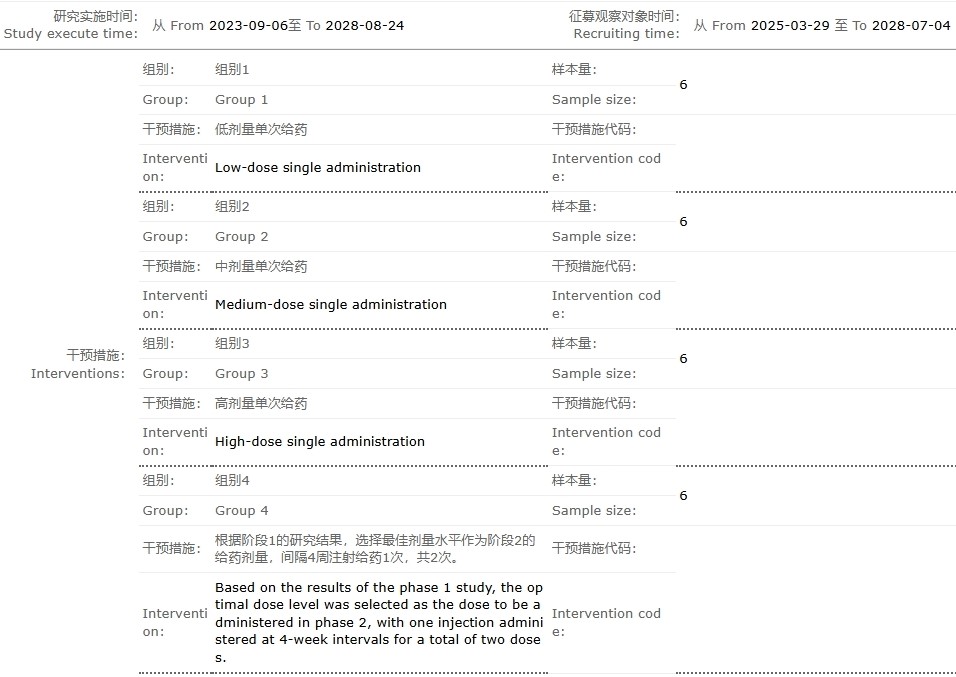
截图来源:中国临床试验注册中心
三、研究指标与期望结果
本研究将重点关注干细胞注射液的剂量限制性毒性(DLT)、不良事件及其安全性。同时,通过勃起硬度分级(EHS)、性生活日记(SEP2和SEP3)及夜间勃起监测(NPTR)的变化,客观评估治疗效果。
专家团队希望通过这项研究,为长期受药物治疗困扰的患者提供一种既安全又有效的全新治疗方案。
四、志愿者招募
-
谁可以参与
参加本次实验的患者需要满足如下条件:
(1)年龄18-60周岁(含18和60周岁),男性;
(2)2型糖尿病血糖控制正常同时合并勃起功能障碍患者;
(3)存在6个月以上病程的中、重度ED(国际勃起功能问卷-5 分数在5至11分之间);
(4)过去3个月内经过规范PDE5i治疗无明显改善;
(5)至少在首次给药前3个月内及本试验过程中有固定的女性性伴侣,且在试验期间期望与该女性性伴侣保持性生活;
(6)同意在试验期间每4周至少尝试4次性交;
(7)试验期间及试验结束后3个月内,同意采取有效的避孕措施;
(8)自愿参加并签署知情同意书。
- 谁不能参与
为了确保试验的安全性,以下患者将被排除:
(1)有明显生殖器结构异常或皮肤感染等局部问题者;
(2)合并性腺功能减退症、心理性ED或严重心脏病史者;
(3)曾接受过骨盆手术、放疗或干细胞治疗者;
(4)合并有肿瘤疾病或既往有肿瘤病史;
(5)肝功能、肾功能异常或感染传染性疾病者;
(6)对试验制剂有过敏反应或存在其他不适合参与试验的情况者。
-
联系方式
✔地址:
上海交通大学医学院附属仁济医院(上海市黄浦区山东中路145号)
✔联系人:
卢慕峻 教授
✔邮箱:
lumujun@163.com
本研究已获“中国临床试验注册中心”(注册号:ChiCTR2500096940)的预注册。将严格按照临床试验规范(GCP)执行。若您对本研究有任何疑问,请进行邮件咨询。期待有“糖友”能够加试验,让干细胞疗法为您的健康与“幸福”添上一份力!
稿件来源:昂昇科研部&临床部


